출처: https:tk//uwspace.uwaterloo.ca/bitstream/handle/10012/8455/Adeosun_David.PDF.pdf?%09sequence=5
4. 화재발생 단계
경질우레탄폼은 화재 발전의 다른 단계 동안 화염 연소 또는 비화염 조건에서 분해될 수 있습니다. 물질이 노출된 온도와 주변 산소 농도는 화재의 단계 동안 상당히 다양해 화재 중 다양한 시간에 생성되는 가스는 그 성격과 농도 모두에서 매우 달라질 수 있습니다. 실제 화재의 다양한 단계에서 생성된 가스는 열분해, 열산성화 및/또는 화염 연소로 인한 것일 수 있지만, 모든 경우에 많은 다른 화합물의 복잡한 혼합물로 구성됩니다. 재료가 실제 화재 상황에 어떻게 반응할 수 있는지 평가하기 위해, 실제 화재 중에 발생하는 조건과 샘플이 화재성능 테스트 중에 적용되는 조건을 관련시키는 것이 중요합니다.
아래 그림에서 열분해, 완전 개발 및 붕괴 단계를 포함하여 화재 발생의 주요 단계에 대한 일반적인 개요를 보여줍니다. 처음부터 화재는 산소가 풍부한 환경에서 열분해가 발생하는 동안 느린 유도 기간으로 시작할 수 있습니다.
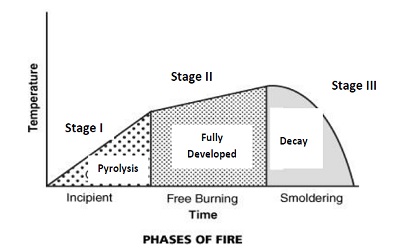
[통풍이 잘되는 구획된 화재의 이상적인 온도–시간 단계]
점화 후, 화재는 산소의 접근성이나 연료의 가용성에 의해 크기가 제한될 때까지 매우 빠르게 성장합니다. 화재 곡선의 모양은 연료 유형, 양 및 표면적, 구획 구조 및 환기 조건과 같은 매개 변수에 따라 다릅니다. 또한 화재 발전의 각 단계마다 고유한 특성이 있으므로, 각 단계에서 재료 분해 및 연소에 난연제의 영향은 가스 생성의 원리를 규명하고 화재 대응 인력의 안전에 미칠 수 있는 영향을 철저히 이해해야합니다.
Alajberg의 연구에서, 디페닐메탈 디이소시아네이트(diphenylmethane diisocyanate, MDI) 및 폴리(oxy-tetramethylene) 글리콜 공중합체로부터 생성된 경질우레탄폼은 화재 발생의 주요 단계를 시뮬레이션하기 위한 온도 및 대기 조건에서 비화염 연소 동안 분해되었습니다. 비 화염 조건은 온도는 시뮬레이션하기 위한 550℃(화재의 시작), 750℃(발화), 950℃(성숙된 화재)로 구성되고, 대기(주변 대기 중의 산소가 정상 공기의 함량과 일치할 때 화재가 시작하거나 좋은 통풍이 존재)는 공기, 공기–질소(1:1)(산소의 절반이 이미 열–산화에 의해 소비되는 상태), 및 질소(산소가 완전히 소비된 상태)를 나타내도록 조절된 산소와 질소의 혼합물로 구성됩니다.
경량 가스, 유기 및 응축성 휘발성 유기화합물을 생성하고, GC-MS(Gas Chromatography/Mass Spectrometry)분석을 사용하여 확인하였습니다. 각 정화(불순하거나 더러운 것을 깨끗하게 함)의 수율은 분해 온도와 주변 대기의 산소 함량에 따라 달라졌습니다. 아래의 표는 연구된 모든 조건에서 일반적인 분해 산물을 보여줍니다. 현재 연구에서, 화재 발달의 각 단계에서 발생하는 조건과 유사한 조건은 다음 섹션에서 논의되는 각 단계의 특성에 기초하여 콘칼로리미터나 연기 밀도 챔버(또는 두 가지 모두)에서 설정됩니다.
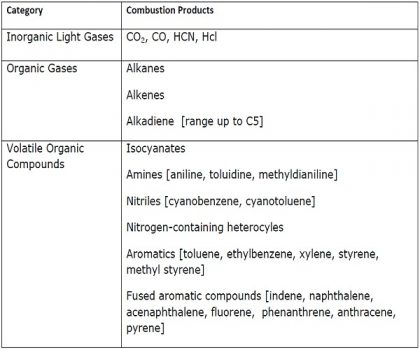
[경질우레탄폼의 비 점화 연소로 인한 가스 생성물]
(1) 1단계: 열산화 열분해(Thermo-oxidative pyrolysis)
화재 조건에 대한 중합체 재료의 노출 1단계는 일반적으로 통풍이 잘되는 조건에서 물질의 열분해를 수반할 수 있으며, 다음에는 추가적인 산화, 점화 및 연소가 밀접하게 따라올 수 있습니다. 일반적으로 말하면, 경질우레탄폼의 열산화 분해는 공기 중에 산소의 존재에서 충분한 열에 노출로 인해 긴 중합체 사슬의 불가역적인 화학적 분열입니다. 초기 연구자들 사이에서 산화와 불할성 대기에서 경질우레탄폼의 일반적인 분해 경로는 세 가지 독립적인 원리의 조합에 의해 발생한다는 것이 확립되었습니다. 그것은 폴리이소시아네이트 와 폴리올에 대한 물질의 1차 분열 반응으로 시작하여 복잡한 일련의 2차 반응이 뒤따릅니다.
분해의 후속적인 중간 원리는 우레탄폼의 특정 구조에 따라 달라지며, 세부 연소 거동 및 생성 또한 환기 및 온도와 같은 다른 조건에 따라 달라집니다. 각 단계에서 제안된 원리는 다음과 같습니다.
ⅰ) 우레탄과 이소시아네이트 및 알콜의 분리
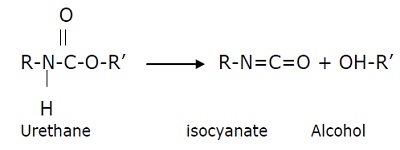
ⅱ) 1차 아민, 올레핀 및 일산화탄소의 분리
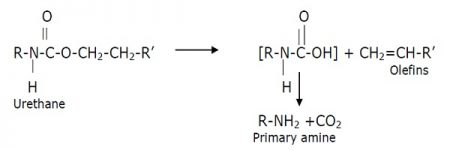
ⅲ) 이산화탄소의 제거, 2차 아민 형성
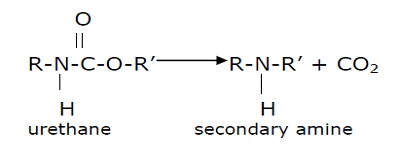
300℃ 질소 대기에서 페닐 이소시아네이트와 1-페닐에탄올의 우레탄 열화 분해 중 3가지 반응이 동시에 발생한 것으로 Dyer는 보고했습니다. 모든 조건에서 발생할 수 있는 2차 반응은 우레아, 알로포네이트, 바이오레트, 이소시아네이트의 트리머 및 카르보디이미드와 같은 생성물 형성을 초래할 수 있습니다. 이소시아네이트 작용기(-NCO)는 질소 함유 분해 생성물의 잠재적인 공급원입니다. 따라서 온도와 높은 O2 농도 조건에서 열분해 또는 화염 연소는 질소 산화물의 생성으로 이어질 것입니다.
Backus 연구진은 산소가 충분한 경우, 우레탄은 이소시아네이트로 분해되지 않고, 독성이 적은 아민, 올레핀 및 O2로 산화된다는 것을 관찰했습니다. 그는 열 중력 분석(TGA), 시차열 분석(DTA)과 숯 및 휘발성 제품의 적외선 분광법을 사용하여 공기 중에 경질 폴리에테르 및 폴리에스테르 기반 경질우레탄폼의 분해를 연구했습니다. 결과는 위에서 언급한 과정과 대체로 일치했으며 공기 중 우레탄폼에 숯 형성이 보다 안정적인 구조로 산화를 수반한다는 것을 나타냈습니다.
특히 고온 조건에서 우레탄 연결 이외의 결합이 깨지고 분해 생성믈의 반응이 발생하기 때문에 발견되는 생성물의 배열은 산소의 존재에서 상당히 증가되었습니다. 난연제 측면에서, Backus는 베이스 폼에 인계 난연제를 도입하면 반응 온도가 낮아져 고체 숯 형성이 향상되고 열 분해시 가연성 제품의 형성이 감소된다는 점을 주목했습니다. 이 연구를 통해 구성이 효과적인 난연제를 형성했음을 시사합니다.
참고로 준불연 경질우레탄폼단열재 간이 화재시험에 대한 시간대별 사진입니다. 5초 간격으로 사진을 계속 올리도록 하겠습니다. 참고하시기 바랍니다.

[준불연 경질우레탄폼단열재 간이 화재시험 준비]
[화재시험 시작]
[5초 경과]
[10초 경과]
[15초 경과]
